Вода — вещество привычное и необычное. Почти 3/4 поверхности нашей
планеты занято океанами и морями. Твёрдой водой — снегом и льдом —
покрыто 20% суши. От воды зависит климат планеты. Геофизики утверждают,
что Земля давно бы остыла и превратилась в безжизненный кусок камня, если бы не вода.
У неё очень большая теплоёмкость. Нагреваясь, она поглощает тепло;
остывая, отдаёт его. Земная вода и поглощает, и возвращает очень много
тепла и тем самым "выравнивает" климат. А от космического холода
предохраняет Землю те молекулы воды, которые рассеяны в атмосфере — в
облаках и в виде паров. Вода – самое загадочное вещество в природе после ДНК,
обладающее уникальными свойствами, которые не только ещё полностью не
объяснены, но далеко не все известны. Чем дольше ее изучают, тем больше
находят новых аномалий и загадок в ней. Большинство из этих аномалий,
обеспечивающих возможность жизни на Земле, объясняются наличием между
молекулами воды водородных связей, которые много сильнее
вандерваальсовских сил притяжения между молекулами других веществ, но на
порядок величины слабее ионных и ковалентных связей между атомами в
молекулах. Такие же водородные связи также присутствуют и в молекуле
ДНК. Молекула воды (H216O) состоит из двух атомов водорода (H) и одного атома кислорода (16O).
Оказывается, что едва ли не все многообразие свойств воды и необычность
их проявления определяется, в конечном счете, физической природой этих
атомов, способом их объединения в молекулу и группировкой образовавшихся
молекул. 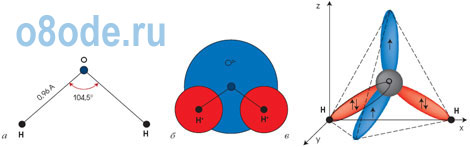
Рис. Строение молекулы воды.
Геометрическая схема (а), плоская модель (б) и пространственная
электронная структура (в) мономера H2O. Два из четырех электронов
внешней оболочки атома кислорода участвуют в создании ковалентных связей
с атомами водорода, а два других образуют сильно вытянутые электронные
орбиты, плоскость которых перпендикулярна плоскости Н-О-Н. Молекула воды H2O
построена в виде треугольника: угол между двумя связками кислород —
водород 104 градуса. Но поскольку оба водородных атома расположены по
одну сторону от кислорода, электрические заряды в ней
рассредоточиваются. Молекула воды полярная, что является причиной
особого взаимодействия между разными её молекулами. Атомы водорода в
молекуле H2O, имея частичный положительный заряд,
взаимодействуют с электронами атомов кислорода соседних молекул. Такая
химическая связь называется водородной. Она объединяет молекулы H2O
в своеобразные ассоциаты пространственного строения; плоскость, в
которой расположены водородные связи, перпендикулярны плоскости атомов
той же молекулы H2O. Взаимодействием между молекулами воды и
объясняются в первую очередь незакономерно высокие температуры её
плавления и кипения. Нужно подвести дополнительную энергию, чтобы
расшатать, а затем разрушить водородные связи. И энергия эта очень
значительна. Вот почему так велика теплоёмкость воды. 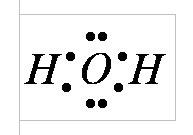 В
молекуле воды имеются две полярные ковалентные связи Н–О. Они
образованы за счёт перекрывания двух одноэлектронных р — облаков атома
кислорода и одноэлектронных S — облаков двух атомов водорода. В
молекуле воды имеются две полярные ковалентные связи Н–О. Они
образованы за счёт перекрывания двух одноэлектронных р — облаков атома
кислорода и одноэлектронных S — облаков двух атомов водорода.
В
соответствии с электронным строением атомов водорода и кислорода
молекула воды располагает четырьмя электронными парами. Две из них
участвуют в образовании ковалентных связей с двумя атомами водорода,
т.е. являются связывающими. Две другие электронные пары являются
свободными - не связывающими. Они образуют электронное облако. Облако
неоднородно – в нем можно различить отдельные сгущения и разрежения. В
молекуле воды имеются четыре полюс зарядов: два — положительные и два —
отрицательные. Положительные заряды сосредоточены у атомов водорода,
так как кислород электроотрицательнее водорода. Два отрицательных полюса
приходятся на две не связывающие электронные пары кислорода. У
кислородного ядра создается избыток электронной плотности. Внутренняя
электронная пара кислорода равномерно обрамляет ядро: схематически она
представлена окружностью с центром -ядром O2-. Четыре внешних
электрона группируются в две электронные пары, тяготеющие к ядру, но
частично не скомпенсированные. Схематически суммарные электронные
орбитали этих пар показаны в виде эллипсов, вытянутых от общего центра –
ядра O2-. Каждый из оставшихся двух электронов кислорода
образует пару с одним электроном водорода. Эти пары также тяготеют к
кислородному ядру. Поэтому водородные ядра – протоны – оказываются
несколько оголенными, и здесь наблюдается недостаток электронной
плотности. 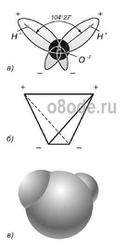 Таким образом, в молекуле воды различают четыре полюса зарядов: два
отрицательных (избыток электронной плотности в области кислородного
ядра) и два положительных (недостаток электронной плотности у двух
водородных ядер). Для большей наглядности можно представить, что полюса
занимают вершины деформированного тетраэдра, в центре которого находится
ядро кислорода. Таким образом, в молекуле воды различают четыре полюса зарядов: два
отрицательных (избыток электронной плотности в области кислородного
ядра) и два положительных (недостаток электронной плотности у двух
водородных ядер). Для большей наглядности можно представить, что полюса
занимают вершины деформированного тетраэдра, в центре которого находится
ядро кислорода.
Рис. Строение молекулы воды: а – угол между связями O-H; б – расположение полюсов заряда; в – внешний вид электронного облака молекулы воды. Почти
шарообразная молекула воды имеет заметно выраженную полярность, так как
электрические заряды в ней расположены асимметрично. Каждая молекула
воды является миниатюрным диполем с высоким дипольным моментом – 1,87
дебая. Дебай – внесистемная единица электрического дипольного 3,33564·1030
Кл·м. Под воздействием диполей воды в 80 раз ослабевают межатомные или
межмолекулярные силы на поверхности погруженного в нее вещества. Иначе
говоря, вода имеет высокую диэлектрическую проницаемость, самую высокую
из всех известных нам соединений. Во многом благодаря этому, вода
проявляет себя как универсальный растворитель. Ее растворяющему
действию в той или иной мере подвластны и твердые тела, и жидкости, и
газы. Удельная теплоемкость воды наибольшая среди всех веществ.
Кроме того, она в 2 раза выше, чем у льда, в то время как у большинства
простых веществ (например, металлов) в процессе плавления теплоемкость
практически не изменяется, а у веществ из многоатомных молекул она, как
правило, уменьшается при плавлении. Подобное представление о
строении молекулы позволяет объяснить многие свойства воды, в частности
структуру льда. В кристаллической решётке льда каждая из молекул
окружена четырьмя другими. В плоскостном изображении это можно
представить так: 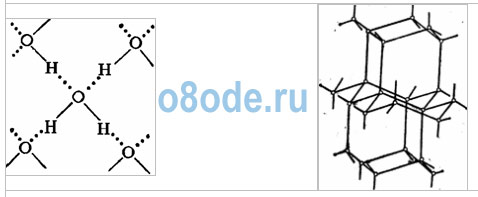
Связь
между молекулами осуществляется посредством атома водорода.
Положительно заряженный атом водорода одной молекулы воды притягивается к
отрицательно заряженному атому кислорода другой молекулы воды. Такая
связь получила название водородной (её обозначают точками). По прочности
водородная связь примерно в 15 — 20 раз слабее ковалентной связи.
Поэтому водородная связь легко разрывается, что наблюдается, например,
при испарении воды. 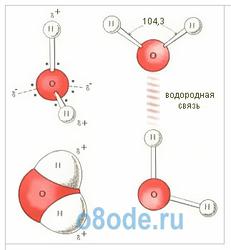 Рис. слева - Водородные связи между молекулами воды Рис. слева - Водородные связи между молекулами воды
Структура
жидкой воды напоминает структуру льда. В жидкой воде молекулы также
связаны друг с другом посредством водородных связей, однако структура
воды менее "жёсткая", чем у льда. Вследствие теплового движения молекул в
воде одни водородные связи разрываются, другие образуются. 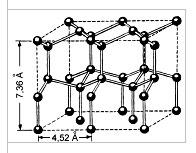
Рис. Кристаллическая решётка льда. Молекулы воды H2O (чёрные шарики) в её узлах расположены так, что каждая имеет четырёх „соседок". Полярность
молекул воды, наличие в них частично нескомпенсированных электрических
зарядов порождает склонность к группировке молекул в укрупненные
«сообщества» – ассоциаты. Оказывается, полностью соответствует формуле
Н2O лишь вода, находящаяся в парообразном состоянии. Это показали
результаты определения молекулярной массы водяного пара. В температурном
интервале от 0 до 100°С концентрация отдельных (мономерных молекул)
жидкой воды не превышает 1%. Все остальные молекулы воды объединены в
ассоциаты различной степени сложности, и их состав описывается общей
формулой (H2O)x. Непосредственной причиной образования
ассоциатов являются водородные связи между молекулами воды. Они
возникают между ядрами водорода одних молекул и электронными
«сгущениями» у ядер кислорода других молекул воды. Правда, эти связи в
десятки раз слабее, чем «стандартные» внутримолекулярные химические
связи, и достаточно обычных движений молекул, чтобы разрушить их. Но под
влиянием тепловых колебаний так же легко возникают и новые связи этого
типа. Возникновение и распад ассоциатов можно выразить схемой: x·H2O↔ (H2O)x Поскольку
электронные орбитали в каждой молекуле воды образуют тетраэдрическую
структуру, водородные связи могут упорядочить расположение молекул воды в
виде тетраэдрических координированных ассоциатов. Большинство
исследователей объясняют аномально высокую теплоемкость жидкой воды тем,
что при плавлении льда его кристаллическая структура разрушается не
сразу. В жидкой воде сохраняются водородные связи между молекулами. В
ней остаются как бы обломки льда - ассоциаты из большого или меньшего
числа молекул воды. Однако в отличие от льда каждый ассоциат существует
недолго. Постоянно происходит разрушение одних и образование других
ассоциатов. При каждом значении температуры в воде устанавливается свое
динамическое равновесие в этом процессе. А при нагревании воды часть
теплоты затрачивается на разрыв водородных связей в ассоциатах. При этом
на разрыв каждой связи расходуется 0,26-0,5 эВ. Этим и объясняется
аномально высокая теплоемкость воды по сравнению с расплавами других
веществ, не образующих водородных связей. При нагревании таких расплавов
энергия расходуется только на сообщение тепловых движений их атомам или
молекулам. Водородные связи между молекулами воды полностью разрываются
только при переходе воды в пар. На правильность такой точки зрения
указывает и то обстоятельство, что удельная теплоемкость водяного пара
при 100°С практически совпадает с удельной теплоемкостью льда при 0°С. Рисунок ниже: Элементарным структурным элементом ассоциата является кластер: Рис. Отдельный гипотетический кластер воды. Отдельные кластеры образуют ассоциаты молекул воды (H2O)x: Рис. Кластеры из молекул воды образуют ассоциаты. 
Существует
и другая точка зрения на природу аномально высокой теплоемкости воды.
Профессор Г. Н. Зацепина заметила, что молярная теплоемкость воды,
составляющая 18 кал/(мольград), точно равна теоретической молярной
теплоемкости твердого тела с трехатомными кристаллами. А в соответствии с
законом Дюлонга и Пти атомные теплоемкости всех химически простых
(одноатомных) кристаллических тел при достаточно высокой температуре
одинаковы и равны 6 калДмоль o град). А для трехатомных, в граммоле
которых содержится 3 Nа узлов кристаллической решетки, - в 3 раза больше. (Здесь Nа - число Авогадро). Отсюда следует, что вода является как бы кристаллическим телом, состоящим из трехатомных молекул Н20.
Это соответствует распространенному представлению о воде как смеси
кристаллоподобных ассоциатов с небольшой примесью свободных молекул H2O
воды между ними, число которых растет с повышением температуры. С этой
точки зрения вызывает удивление не высокая теплоемкость жидкой воды, а
низкая твердого льда. Уменьшение удельной теплоемкости воды при
замерзании объясняется отсутствием поперечных тепловых колебаний атомов в
жесткой кристаллической решетке льда, где у каждого протона,
обуславливающего водородную связь, остается только одна степень свободы
для тепловых колебаний вместо трех. Но за счет чего и как могут
происходить столь большие изменения теплоемкости воды без
соответствующих изменений давления? Чтобы ответить на этот вопрос,
познакомимся с гипотезой кандидата геолого-минералогических наук Ю. А. Колясникова о структуре воды.
Он указывает, что еще первооткрыватели водородных связей Дж. Бернал и
Р. Фаулер в 1932 г. сравнивали структуру жидкой воды с кристаллической
структурой кварца, а те ассоциаты, о которых говорилось выше, - это в
основном тетрамеры 4Н20, в которых четыре молекулы воды
соединены в компактный тетраэдр с двенадцатью внутренними водородными
связями. В результате образуется четырёхгранная пирамида - тетраэдр. При
этом, водородные связи в этих тетрамерах могут образовывать как право-
так и левовинтовую последовательности, подобно тому, как кристаллы
широко распространённого кварца (Si02), тоже имеющие
тетраэдрическую структуру, бывают право- и лево-вращательной
кристаллической форм. Поскольку каждый такой тетрамер воды имеет еще и
четыре незадействованные внешние водородные связи (как у одной молекулы
воды), то тетрамеры могут соединяться этими внешними связями в своего
рода полимерные цепочки, наподобие молекулы ДНК. А поскольку внешних
связей всего четыре, а внутренних - в 3 раза больше, то это позволяет
тяжелым и прочным тетрамерам в жидкой воде изгибать, поворачивать и даже
надламывать эти ослабленные тепловыми колебаниями внешние водородные
связи. Это и обуславливает текучесть воды.
Такую структуру
вода, по мнению Колясникова, имеет только в жидком состоянии и,
возможно, частично в парообразном. А вот во льду, кристаллическая
структура, которого хорошо изучена, тетрагидроли соединены между собой
негибкими равнопрочными прямыми водородными связями в ажурный каркас с
большими пустотами в нем, что делает плотность льда меньше плотности
воды.  Рис. Кристаллическая структура льда: молекулы воды соединены в правильные шестиугольники Рис. Кристаллическая структура льда: молекулы воды соединены в правильные шестиугольники
Когда
же лед тает, часть водородных связей в нем ослабевает и изгибается, что
ведет к перестройке структуры в вышеописанные тетрамеры и делает жидкую
воду более плотной, чем лед. При 4°С наступает состояние, когда все
водородные связи между тетрамерами максимально изогнуты, чем и
обуславливается максимум плотности воды при этой температуре. Дальше
связям гнуться некуда.
При температуре выше 4°С начинается
разрывание отдельных связей между тетрамерами, и при 36-37°С оказывается
разорвана половина внешних водородных связей. Это и определяет минимум
на кривой зависимости удельной теплоемкости воды от температуры. При
температуре же 70°С разорваны уже почти все межтетрамерные связи, и
наряду со свободными тетрамерами в воде остаются только короткие обрывки
"полимерных" цепочек из них. Наконец при кипении воды происходит
окончательный разрыв теперь уже одиночных тетрамеров на отдельные
молекулы Н20. И то обстоятельство, что удельная теплота
испарения воды ровно в 3 раза больше суммы удельных теплот плавления
льда и последующего нагрева воды до 100°С, является подтверждением
предположения Колясникова о том. что число внутренних связей в тетрамере
в 3 раза больше числа внешних.
Такая тетраэдрально-винтовая
структура воды может быть обусловлена ее древней реологической связью с
кварцем и другими кремнекислородными минералами, преобладающими в земной
коре, из недр которой когда-то появилась вода на Земле. Как маленький
кристаллик соли заставляет окружающий его раствор кристаллизоваться в
подобные ему кристаллы, а не в другие, так кварц заставил молекулы воды
выстраиваться в тетраэдрические структуры, которые, энергетически
наиболее выгодны. А в нашу эпоху в земной атмосфере водяные пары,
конденсируясь в капли, образуют такую структуру потому, что в атмосфере
всегда присутствуют мельчайшие капельки аэрозольной воды, уже имеющей
эту структуру. Они и являются центрами конденсации водяных паров в
атмосфере. Ниже приведены возможные цепочечные силикатные структуры на
основе тетраэдра, которые могут быть составлены и из тетраэдров воды. Рис. Элементарный правильный кремне-кислородный тетраэдр SiO44-. Рис. Элементарные кремнекислородные единицы-ортогруппы SiO44- в структуре Mg-пироксена энстатите (а) и диортогруппы Si2 O76- в Са-пироксеноиде волластоните (б). 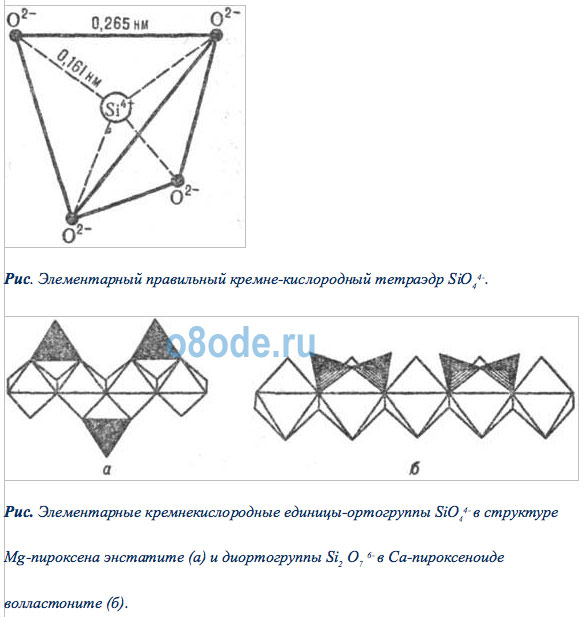
Рис. Простейшие типы островных кремнекислородных анионных группировок: а-SiO4, б-Si2O7, в-Si3O9, г-Si4О12, д-Si6O18. 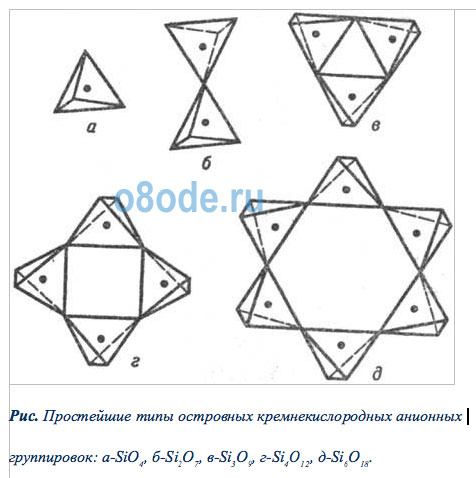
Рис.
ниже - Важнейшие типы кремнекислородных цепочечных анионных группировок
(по Белову): а-метагерманатная, б - пироксеновая, в - батиситовая,
г-волластонитовая, д-власовитовая, е-мелилитовая, ж-родонитовая,
з-пироксмангитовая, и-метафосфатная, к-фторобериллатная, л -
барилитовая. 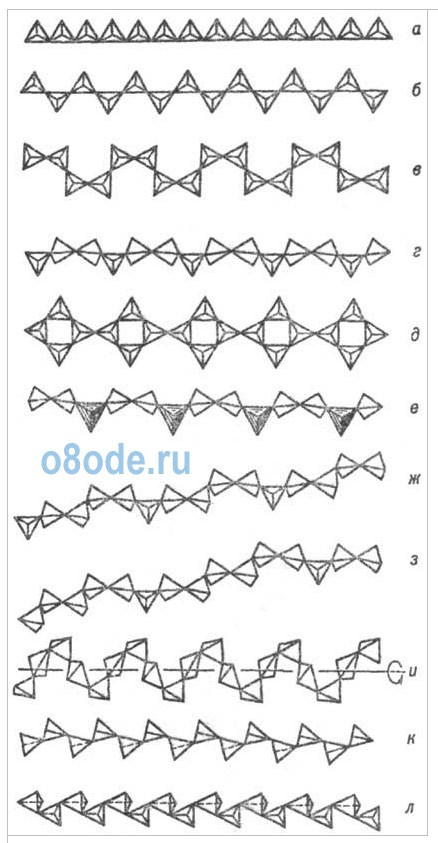
Рис.
ниже - Конденсация пироксеновых кремнекислородных анионов в сотовые
двухрядные амфиболовые (а), трехрядные амфиболоподобные (б), слоистые
тальковые и близкие им анионы (в). 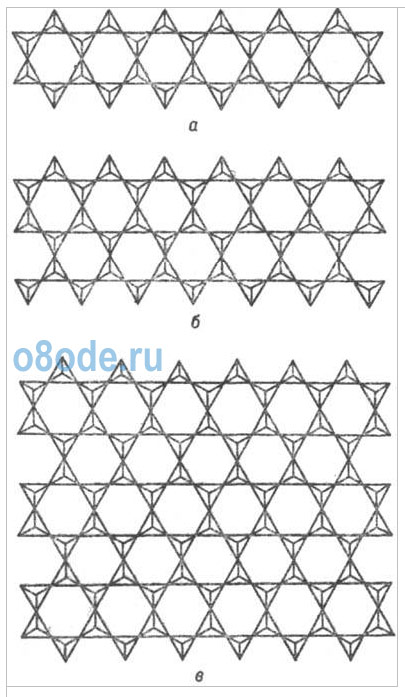
Рис.
ниже - Важнейшие типы ленточных кремнекислородных группировок (по
Белову): а - силлиманитовая, амфиболовая, ксонотлитовая;
б-эпидидимитовая; в-ортоклазовая; г-нарсарсукитовая; д-фенакитовая
призматическая; е-эвклазовая инкрустированная. 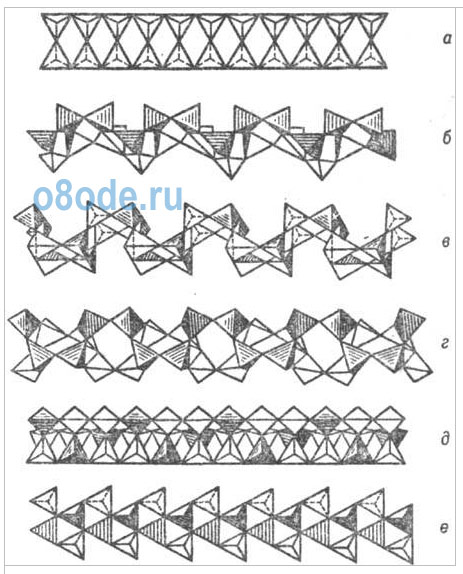
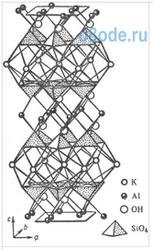 Рис. справа - Фрагмент (элементарный пакет) слоистой кристаллической структуры мусковита KAl2(AlSi3O10XOH)2,
иллюстрирующий переслаивание алюмокремне-кислородных сеток с
полиэдрическими слоями крупных катионов алюминия и калия, напоминает
цепочку ДНК. Рис. справа - Фрагмент (элементарный пакет) слоистой кристаллической структуры мусковита KAl2(AlSi3O10XOH)2,
иллюстрирующий переслаивание алюмокремне-кислородных сеток с
полиэдрическими слоями крупных катионов алюминия и калия, напоминает
цепочку ДНК.
Возможны и другие модели водной структуры.
Тетраэдрически связанные молекулы воды образуют своеобразные цепочки
довольно стабильного состава. Исследователи раскрывают все более тонкие
и сложные механизмы «внутренней организации» водной массы. Кроме
льдоподобной структуры, жидкой воды и мономерных молекул, описан и
третий элемент структуры – нететраэдрической. Определенная часть
молекул воды ассоциирована не в трехмерные каркасы, а в линейные
кольцевые объединения. Кольца, группируясь, образуют еще более сложные
комплексы ассоциатов. Таким образом, вода теоретически может
образовывать цепочки, наподобие молекулы ДНК, о чём будет сказано ниже. В
этой гипотезе интересно еще и то, что из нее следует равновероятность
существования право - и левовинтовой воды. Но биологами давно подмечено,
что в биологических тканях и структурах наблюдаются только либо лево -,
либо правовинтовые образования. Пример тому - белковые молекулы,
построенные только из лево-винтовых аминокислот и закрученные только по
левовинтовой спирали. А вот сахара в живой природе - все только
правовинтовые. Никто пока не смог объяснить, почему в живой природе
обнаруживается такое предпочтение к левому в одних случаях и к правому -
в других. Ведь в неживой природе с равной вероятностью встречаются как
право-, так и левовинтовые молекулы. Более ста лет назад
знаменитый французский естествоиспытатель Луи Пастер обнаружил, что
органические соединения в составе растений и животных оптически
асимметричны - они вращают плоскость поляризации падающего на них света.
Все аминокислоты, входящие в состав животных и растений, вращают
плоскость поляризации влево, а все сахара - вправо. Если мы синтезируем
такие же по химическому составу соединения, то в каждом из них будет
равное количество лево- и правовращающих молекул. Как известно,
все живые организмы состоят из белков, а они, в свою очередь, - из
аминокислот. Соединяясь друг с другом в разнообразной
последовательности, аминокислоты образуют длинные пептидные цепи,
которые самопроизвольно "закручиваются" в сложные белковые молекулы.
Подобно многим другим органическим соединениям, аминокислоты обладают
хиральной симметрией (от греч. хирос - рука), то есть могут существовать
в двух зеркально симметричных формах, называемых "энантиомеры". Такие
молекулы похожи одна на другую, как левая и правая рука, поэтому их
называют D- и L-молекулами (от лат. dexter, laevus - правый и левый). 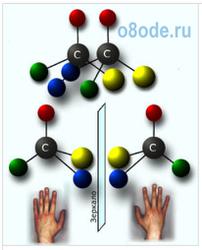 Теперь
представим себе, что среда с левыми и правыми молекулами перешла в
состояние только с левыми или только с правыми молекулами. Такую среду
специалисты называют хирально (от греческого слова "хейра" - рука)
упорядоченной. Самовоспроизведение живого (биопоэз - по определению Д.
Бернала) могло возникнуть и поддерживаться только в такой среде. Теперь
представим себе, что среда с левыми и правыми молекулами перешла в
состояние только с левыми или только с правыми молекулами. Такую среду
специалисты называют хирально (от греческого слова "хейра" - рука)
упорядоченной. Самовоспроизведение живого (биопоэз - по определению Д.
Бернала) могло возникнуть и поддерживаться только в такой среде.
Рис. Зеркальная симметрия в природе Другое
название молекул-энантиомеров - "правовращающие" и "левовращающие" -
происходит от их способности вращать плоскость поляризации света в
различных направлениях. Если линейно поляризованный свет пропустить
через раствор таких молекул, происходит поворот плоскости его
поляризации: по часовой стрелке, если молекулы в растворе правые, и
против - если левые. А в смеси одинаковых количеств D-и L-форм (она
называется "рацемат") свет сохранит первоначальную линейную поляризацию.
Это оптическое свойство хиральных молекул впервые было обнаружено Луи
Пастером в 1848 году. Любопытно, что почти все природные белки
состоят только из левых аминокислот. Этот факт тем более удивляет, что
при синтезе аминокислот в лабораторных условиях образуется примерно
одинаковое число правых и левых молекул. Оказывается, этой особенностью
обладают не только аминокислоты, но и многие другие важные для живых
систем вещества, причем каждое имеет строго определенный знак зеркальной
симметрии во всей биосфере. Например, сахара, входящие в состав многих
нуклеотидов, а также нуклеиновых кислот ДНК и РНК, представлены в
организме исключительно правыми D-молекулами. Хотя физические и
химические свойства "зеркальных антиподов" совпадают, их физиологическая
активность в организмах различна: L-caxaра не усваиваются,
L-фенилаланин в отличие от безвредных его D-молекул вызывает психические
заболевания и т. д. Согласно современным представлениям о
происхождении жизни на Земле, выбор органическими молекулами
определенного типа зеркальной симметрии послужил главной предпосылкой их
выживания и последующего самовоспроизводства. Однако вопрос, как и
почему произошел эволюционный отбор того или иного зеркального антипода,
- до сих пор остается одной из самых больших загадок науки. Советский
ученый Л. Л. Морозов доказал, что переход к хиральной упорядоченности
мог произойти не эволюционно, а только при каком-то определённом резком
фазовом изменении. Академик В. И. Гольданский назвал этот переход,
благодаря которому зародилась жизнь на Земле хиральной катастрофой. Как же возникли условия для фазовой катастрофы, вызвавшей хиральный переход? Наиболее
важным было то, что органические соединения плавились при 800-1000 0С в
земной коре, а верхние остывали до температуры космоса, то есть
абсолютного нуля. Перепад температуры достигал 1000 °С. В таких условиях
органические молекулы плавились под действием высокой температуры и
даже полностью разрушались, а верх оставался холодным, так как
органические молекулы замораживались. Газы и пары воды, которые
просачивались из земной коры, меняли химический состав органических
соединений. Газы несли с собой тепло, из-за чего граница плавления
органического слоя смещалась вверх и вниз, создавая градиент. При
очень низких давлениях атмосферы вода была на земной поверхности лишь в
виде пара и льда. Когда же давление достигало так называемой тройной
точки воды (0,006 атмосферы), вода впервые смогла находиться в виде
жидкости. Конечно, лишь экспериментально можно доказать, что
именно вызвало хиральный переход: земные или космические причины. Но так
или иначе в какой-то момент хирально упорядоченные молекулы (а именно -
левовращающие аминокислоты и правовращающие сахара) оказались более
устойчивыми и начался неостановимый рост их количества - хиральный
переход. Летопись планеты повествует и о том, что тогда на Земле
не было ни гор, ни впадин. Полурасплавленная гранитная кора представляла
собой поверхность столь же ровную, как уровень современного океана.
Однако в пределах этой равнины все же были понижения из-за
неравномерного распределения масс внутри Земли. Эти понижения сыграли
чрезвычайно важную роль. Дело в том, что плоскодонные впадины
поперечником в сотни и даже тысячи километров и глубиной не более ста
метров, вероятно, и стали колыбелью жизни. Ведь в них стекала вода,
собиравшаяся на поверхности планеты. Вода разбавляла хиральные
органические соединения в пепловом слое. Постепенно менялся химический
состав соединения, стабилизировалась температура. Переход от неживого к
живому, начавшийся в безводных условиях, продолжался уже в водной среде. Таков
ли сюжет зарождения жизни? Вероятнее всего, что да. В геологическом
разрезе Исуа (Западная Гренландия), возраст которого 3,8 миллиарда лет,
найдены бензино- и нефтеподобные соединения с изотопным соотношением
С12/С13, свойственным углероду фотосинтетического происхождения. Если
биологическая природа углеродистых соединений из разреза Исуа
подтвердится, то получится, что весь период зарождения жизни на Земле -
от возникновения хиральной органики до появления клетки, способной к
фотосинтезу и размножению,- был пройден лишь за сто миллионов лет. И в
этом процессе огромную роль сыграли молекулы воды и ДНК. Самое
удивительное в структуре воды заключается в том, что молекулы воды при
низких отрицательных температурах и высоких давлениях внутри нанотрубок
могут кристаллизоваться в форме двойной спирали, напоминающую ДНК.
Это было доказано компьютерными экспериментами американских учёных под
руководством Сяо Чэн Цзэна в Университете штата Небраска (США). 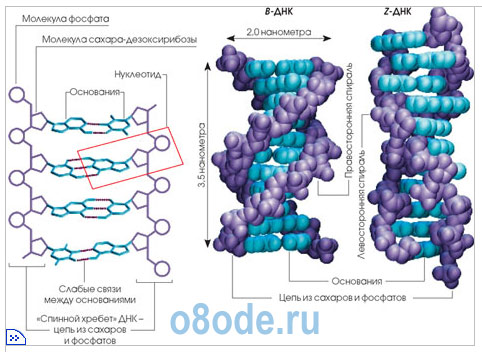
ДНК представляет собой двойную цепочку, скрученную в спираль. Каждая
нить состоит из "кирпичиков" - из последовательно соединенных
нуклеотидов. Каждый нуклеотид ДНК содержит одно из четырёх азотистых
оснований - гуанин (G), аденин (A) (пурины), тимин (T) и цитозин (C)
(пиримидины), связанное с дезоксирибозой, к последней, в свою очередь,
присоединена фосфатная группа. Между собой соседние нуклеотиды соединены
в цепи фосфодиэфирной связью, образованной 3'-гидроксильной (3'-ОН) и
5'-фосфатной группами (5'-РО3). Это свойство обуславливает наличие
полярности в ДНК, т.е. противоположной направленности, а именно 5'- и
3'-концов: 5'-концу одной нити соответствует 3'-конец второй нити.
Последовательность нуклеотидов позволяет «кодировать» информацию о
различных типах РНК, наиболее важными из которых являются
информационные, или матричные (мРНК), рибосомальные (рРНК) и
транспортные (тРНК). Все эти типы РНК синтезируются на матрице ДНК за
счёт копирования последовательности ДНК в последовательность РНК,
синтезируемой в процессе транскрипции и принимают участие в важнейшем
процессе жизни – передачи и копирования информации (трансляции). 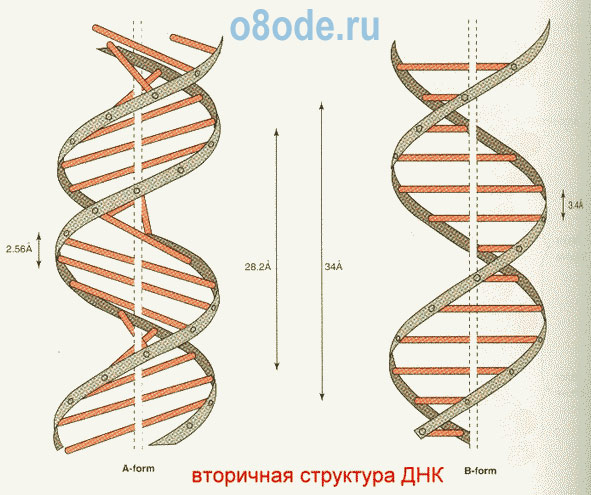
Первичная
структура ДНК - это линейная последовательность нуклеотидов ДНК в цепи.
Последовательность нуклеотидов в цепи ДНК записывают в виде буквенной
формулы ДНК: например - AGTCATGCCAG, запись ведется с 5'- на 3'-конец
цепи ДНК. Вторичная структура ДНК образуется за счет
взаимодействий нуклеотидов (в большей степени азотистых оснований) между
собой, водородных связей. Классический пример вторичной структуры ДНК -
двойная спираль ДНК. Двойная спираль ДНК - самая распространенная в
природе форма ДНК, состоящая из двух полинуклеотидных цепей ДНК.
Построение каждой новой цепи ДНК осуществляется по принципу
комплементарности, т.е. каждому азотистому основанию одной цепи ДНК
соответствует строго определенное основание другой цепи: в
комплемнтарной паре напротив A стоит T, а напротив G располагается C и
т.д. Чтобы вода сформировала спираль, наподобие, в моделируемом
эксперименте она "помещалась" в нанотрубки под высоким давлением,
варьирующимися в разных опытах от 10 до 40000 атмосфер. После этого
задавали температуру, которая имела значение -23°C. Запас по сравнению с
температурой замерзания воды делался в связи с тем, что с повышением
давления температура плавления водяного льда понижается. Диаметр
нанотрубок составлял от 1,35 до 1,90 нм. 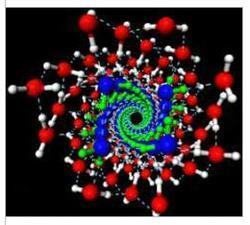 Рис. Общий вид структуры воды (изображение New Scientist) Рис. Общий вид структуры воды (изображение New Scientist)
Молекулы
воды связываются между собой посредством водородных связей, расстояние
между атомами кислорода и водорода равно 96 пм, а между двумя водородами
- 150 пм. В твёрдом состоянии атом кислорода участвует в образовании
двух водородных связей с соседними молекулами воды. При этом отдельные
молекулы H2O соприкасаются друг с другом разноимёнными
полюсами. Таким образом, образуются слои, в которых каждая молекула
связана с тремя молекулами своего слоя и одной из соседнего. В
результате, кристаллическая структура льда состоит из шестигранных
"трубок" соединенных между собой, как пчелиные соты.  Рис. Внутренняя стенка структуры воды (изображение New Scientist) Рис. Внутренняя стенка структуры воды (изображение New Scientist)
Учёные
ожидали увидеть, что вода во всех случаях образует тонкую трубчатую
структуру. Однако, модель показала, что при диаметре трубки в 1,35 нм и
давлении в 40000 атмосфер водородные связи искривились, приведя к
образованию спирали с двойной стенкой. Внутренняя стенка этой структуры
является скрученной в четверо спиралью, а внешняя состоит из четырёх
двойных спиралей, похожих на структуру молекулы ДНК. Последний
факт накладывает отпечаток не только на эволюцию наших представлений о
воде, но и эволюцию ранней жизни и самой молекулы ДНК. Если
предположить, что в эпоху зарождения жизни криолитные глинистые породы
имели форму нанотрубок, возникает вопрос - не могла ли вода,
сорбированная в них служить структурной основой (матрицей) для синтеза
ДНК и считывания информации? Возможно, поэтому спиральная структура ДНК
повторяет спиральную структуру воды в нанотрубках. Как сообщает
журнал New Scientist, теперь нашим зарубежным коллегам предстоит
подтвердить существование таких макромолекул воды в реальных
экспериментальных условиях с использованием инфракрасной спектроскопии и
спектроскопии нейтронного рассеяния.
К.х.н. О.В. Мосин
Источник: http://hhttp://www.o8ode.ru/article/water/voda_i_dnk.htm | 


